-
Sua Malvagità.
User deleted
Aiuto per i compiti - chiedete qui una mano per finire i compiti
Avete saltato dei giorni di scuola e qualcosa non vi è chiaro? State provando da ore a risolvere una disequazione logartimica e non riuscite mai a trovarvi col risultato? Il vostro prof. è un caprone e quando parla non riuscite a capire gli argomenti che spiega? No problem! Dopotutto si sa, la collaborazione è la chiave del successo! Può accadere che qualcuno sia portato per la chimica, altri per la grammatica, altri per l' inglese e alcuni per la matematica, quindi è normale incappare in diffcoltà. In questo topic potrete postare tutti gli esercizi che vi risultano più ostici o meno chiari. Magari quello che per voi risulta impossibile, per qualcun altro è una bazzecola!
Edited by -Matteo- - 27/3/2017, 21:36. -
.
aggiornati il titolo ed il testo del topic: buona fortuna a tutti coloro che avranno bisogno di una mano . -
~Gohan~.
User deleted
Domani ho il compito di matematica e, anche se sono bravo, avrei bisogno di qualcuno che mi aiuta. Gli argomenti del compito sono i radicali, il cerchio e la circonferenza. La prof non sa spiegare e, se qualcuno è disponibile, possiamo parlare per mp. . -
Sua Malvagità.
User deleted
Posta pure qui gli esercizi su cui hai difficoltà così da accogliere pareri più preparati^^ . -
~Gohan~.
User deleted
In realtà non devo fare dei compiti per casa ma devo prepararmi per un compito di matematica che farò domani in classe. Devo ripetere i radicali ma la prof ha detto di non fare direttamente il calcolo e di trasformare il numero prima in una potenza.
Es. ∛8=∛2^3=2
Il problema è che non ricordo se, quando semplifico la radice con i numeri sotto radice, devo dividere o sottrarre(io mi ricordo che si deve dividere).
Se qualcuno riesce a risolvere queste radice utilizzando il metodo sopra indicato in modo da capire meglio come si deve fare.
1)∛96
2)∜243
3)∛33/160 ---> non è una divisione ma una frazione
4)√72/25 ---> non è una divisione ma una frazione. -
.
Premessa, DarkJolly ti ho cancellato il messaggio perchè era puro flood e questo non è assolutamente il topic giusto.
In realtà i problemi sono molto semplici. Considera che metto le potenze in frazione per intendere la radice con indice pari al denominatore (cioè 1/3 è la radice cubica)
1) Consideriamo 96:
- 96 : 2 = 48
- 48 : 2 = 24
- 24 : 2 = 12
- 12 : 2 = 6
- 6 : 2 = 3
- 3 : 3 = 1
Quindi 96=(2^5)*(3). Quindi (96)^(1/3) = (2)*[(2^2*3)^(1/3)] = (2)*[(12)^(1/3)]
2)
- 243 : 3 = 81
- 81 : 3 = 27
- 27 : 3 = 9
- 9 : 3 = 3
- 3 : 3 = 1
Quindi 243=3^5. Quindi (243)^(1/4) = 3*[(3)^(1/4)]
3)
- 33 : 3 = 11
- 11 : 11 = 1
- 160 : 2 = 80
- 80 : 2 = 40
- 40 : 2 = 20
- 20 : 2 = 10
- 10 : 2 = 5
- 5 : 5 = 1
Quindi 33/160 = (3*11)/[(2^5)*(5)]. Faccio la radice cubica ed ottengo (3*11)^(1/3)/{2*[(2^2)*5]^(1/3)} = 1/2 * (33/20)^(1/3)
4)
- 72 : 2 = 36
- 36 : 2 = 18
- 18 : 2 = 9
- 9 : 3 = 3
- 3 : 3 = 3
- 25 : 5 = 5
- 5 : 5 = 1
Quindi 72/25 = (2^3 * 3^2)/(5^2). Ne faccio la radice quadrata ed ottengo {(2*3)*[2^(1/2)]} / 5, cioè 6/5 * 2^(1/2)
Edited by M a r k u s ~ - 2/4/2017, 21:06. -
.
NB: "frazione" e "divisione" sono la stessa cosa, è solo un modo di scriverlo diverso 
Per semplificare una radice, devi dividere l'esponente del radicando e quello del radicale con uno stesso valore. Oppure se possibile (e più semplicemente) si divide l'esponente del radicando con quello del radicale.SPOILER (clicca per visualizzare)
Infatti se avessi ∜(32) posso dividere l'esponente del 3 (ossia il 2) e l'esponente della radice (ossia 4) per 2. In questo modo ottengo √3 (infatti nelle radici semplici ("√") si sottintende l'esponente 2, mentre 31=3)
Inoltre puoi sfruttare la proprietà delle potenze che dice in generale: AmxAn=Am+n. Usando i numeri, puoi trasformare per esempio 27 in 23x24, visto che "7=3+4".
Quindi se per caso avessi ∜(27), puoi scriverlo anche ∜(24x23). A suo volta la radice puoi "spartirla" a entrambi i fattori, ottenendo ∜(24) x ∜(23).
Come vedi nel primo fattore gli esponenti di radicale e radicando sono entrambi 4, quindi possono semplificarsi essere semplificati. Alla fine del tutto ci rimane 2 x ∜(23).
Flashato da Mark, ma spero che due risposte siano meglio di una .
. -
~Gohan~.
User deleted
Io avevo capito abbastanza questo argomento ma, anche per colpa della prof che non sa spiegare nulla, alcune cose non mi erano chiare. Ho cercato su youtube e iniziato a capire come dovevo fare e grazie a voi due ora sono pronto per il compito 
P.S. so che la frazione e la divisione sono la stessa. -
Sua Malvagità.
User deleted
Facci sapere come è andata! . -
.
Scusate domani ho il compito di Chimica e sono in crisi in quanto ho saltato le ultime tre lezione (  ) .
) .
1- Qualcuno mi puo spiegare cosa è un anione e un catione?
Sul libro non c'è niente e la prof su una scheda che ci ha dato in preparazione alla verifica ha fatto una domanda riguardante quelle cose :/ .
2- Cosa diavolo é la struttura di Lewis?. -
.
Allora, penso proprio che sul libro ci debba essere necessariamente qualcosa sui cationi o anioni o temo che non sia un libro di chimica o che tu abbia sbagliato materia xD
Partiamo dall'inizio, sai cos'è uno Ione? Altrimenti non si può proseguire oltre.
Uno Ione è un Atomo o un insieme di Atomi [una Molecola] che non è elettricamente neutro, ovvero avrà una Carica Positiva o una Carica Negativa su di esso.
Come fanno gli Atomi o le Molecole in generale a trasformarsi in Ioni? Facile, perdendo gli Elettroni che sono presenti attorno al loro Nucleo centrale. Come forse saprai gli elementi costituenti la cellula sono
-Protoni e Neutroni, i quali sono presenti all'interno del Nucleo e quindi non possono essere scambiati all'esterno
-Elettroni, i quali invece sono presenti negli Orbitali attorno al Nucleo e potranno essere donati [totalmente o parzialmente] alle altre molecole.
Una molecola positiva, o atomo, [ovvero una molecola che avrà donato un elettrone] è detta Catione [Ricorda che P di positiva viene dopo N, quindi va con C di catione che viene dopo Anione]. Un esempio di Catione è Na+ ovvero una molecola di Sodio che ha donato il proprio unico elettrone esterno.
Una molecola negativa invece è detta Anione, un esempio è il Cloro che acquista un elettrone dal Sodio.
Avete fatto la regola dell'ottetto? Immagino di si, con essa potrai spiegarti facilmente perché Sodio e Cloro sentono la necessità di interagire elettronicamente
Sulla struttura di lewis non sai niente proprio? detta così è un macello xD. -
.
Struttura di Lewis, da quel che ricordo dalle superiori è solo un modo di rappresentare un atomo.. Ecco qua una tabella per esempio: 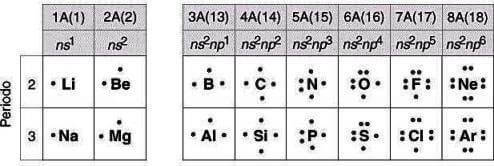
I "pallini" che vedi intorno alla sigla dell'elemento sono gli elettroni situati all'orbitale più esterno (quello non completo), come ben sai in ogni orbitale sono presenti 8 elettroni (tranne nel primo che è formato da due)..
Non c'è molto da dire xD
Ti faccio degli esempi guardando la tabella.
Il Litio (Li) ha 3 elettroni, si trova nel 1° gruppo quindi ha solo un elettrone (di valenza) nell'orbitale esterno, per questo viene rappresentato con un pallino a fianco.
Il Berillio (Be) ha 4 elettroni, si trova nel 2° gruppo quindi ha solo 2 elettroni di valenza, per questo viene rappresentato con 2 pallini a fianco.
Il Sodio (Na) ha invece 11 elettroni (2 + 8 + 3), trovandosi nel 1° gruppo ha solo un elettrone di valenza e quindi un pallino fuori.
Il Carbonio (C) ha 6 elettroni (2 + 4) Quindi 4 pallini attorno..
E così via .
. -
.
Grazie mille ad entrambi  .
.
Comunque no, non c'è niente sul libro, nel paragrafo sugli ioni, li chiama semplicemente ioni positivi e ioni negativo.
Speriamo bene per la verifica .
.
.
. -
.
Come è andata? D: . -
.Grazie mille ad entrambi
 .
.
Comunque no, non c'è niente sul libro, nel paragrafo sugli ioni, li chiama semplicemente ioni positivi e ioni negativo.
Sono solo sinonimi di Cationi ed Anioni, ma è la stessa cosa. Comunque speriamo ti sia andata bene .
.
Supporto Compiti: chiedete qui aiuto per i compitiPerchè la Collaborazione è la chiave del successo! Chiedete qui tutto l'aiuto che vi serve |